पेप्टाइड्स हा संयुगांचा एक वर्ग आहे जो पेप्टाइड बाँडद्वारे अनेक अमीनो ऍसिडच्या जोडणीद्वारे तयार होतो.ते सजीवांमध्ये सर्वव्यापी आहेत.आत्तापर्यंत, सजीवांमध्ये हजारो पेप्टाइड्स सापडले आहेत.पेप्टाइड्स विविध प्रणाली, अवयव, ऊती आणि पेशींच्या कार्यात्मक क्रियाकलापांचे नियमन करण्यासाठी आणि जीवन क्रियाकलापांमध्ये महत्त्वपूर्ण भूमिका बजावतात आणि बहुतेकदा कार्यात्मक विश्लेषण, प्रतिपिंड संशोधन, औषध विकास आणि इतर क्षेत्रांमध्ये वापरले जातात.जैवतंत्रज्ञान आणि पेप्टाइड संश्लेषण तंत्रज्ञानाच्या विकासासह, अधिकाधिक पेप्टाइड औषधे क्लिनिकमध्ये विकसित आणि लागू केली गेली आहेत.
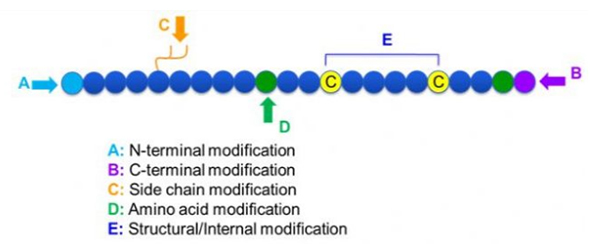
पेप्टाइड बदलांचे विविध प्रकार आहेत, ज्यांना फक्त पोस्ट मॉडिफिकेशन आणि प्रोसेस फेरफार (व्युत्पन्न अमीनो ऍसिड बदल वापरून) आणि एन-टर्मिनल फेरबदल, सी-टर्मिनल बदल, साइड चेन मॉडिफिकेशन, एमिनो ऍसिड मॉडिफिकेशन, स्केलेटन मॉडिफिकेशन, मध्ये विभागले जाऊ शकते. इ., बदल साइटवर अवलंबून (आकृती 1).पेप्टाइड चेनची मुख्य साखळी रचना किंवा साइड चेन गट बदलण्याचे महत्त्वाचे साधन म्हणून, पेप्टाइड बदल पेप्टाइड संयुगांचे भौतिक आणि रासायनिक गुणधर्म प्रभावीपणे बदलू शकतात, पाण्याची विद्राव्यता वाढवू शकतात, व्हिव्होमधील क्रिया कालावधी वाढवू शकतात, त्यांचे जैविक वितरण बदलू शकतात, इम्युनोजेनिकता दूर करू शकतात. , विषारी साइड इफेक्ट्स कमी करा इ. या पेपरमध्ये, अनेक प्रमुख पेप्टाइड सुधारणा धोरणे आणि त्यांची वैशिष्ट्ये सादर केली आहेत.
1. सायकलीकरण
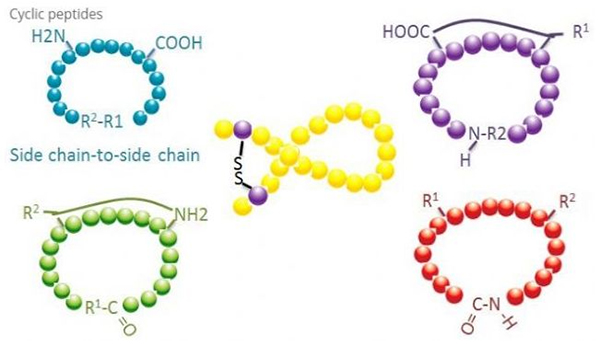
बायोमेडिसिनमध्ये चक्रीय पेप्टाइड्सचे बरेच उपयोग आहेत आणि जैविक क्रियाकलाप असलेले अनेक नैसर्गिक पेप्टाइड्स हे चक्रीय पेप्टाइड्स आहेत.कारण चक्रीय पेप्टाइड्स रेखीय पेप्टाइड्सपेक्षा अधिक कठोर असतात, ते पचनसंस्थेला अत्यंत प्रतिरोधक असतात, पचनसंस्थेत टिकून राहू शकतात आणि लक्ष्य रिसेप्टर्ससाठी मजबूत आत्मीयता प्रदर्शित करतात.सायकलीकरण हा चक्रीय पेप्टाइड्सचे संश्लेषण करण्याचा सर्वात थेट मार्ग आहे, विशेषत: मोठ्या संरचनात्मक कंकाल असलेल्या पेप्टाइड्ससाठी.सायक्लायझेशन मोडनुसार, ते साइड चेन-साइड चेन प्रकार, टर्मिनल - साइड चेन प्रकार, टर्मिनल - टर्मिनल प्रकार (एंड टू एंड प्रकार) मध्ये विभागले जाऊ शकते.
(1) साइडचेन-टू-साइडचेन
साइड-चेन ते साइड-चेन सायकलायझेशनचा सर्वात सामान्य प्रकार म्हणजे सिस्टीन अवशेषांमधील डायसल्फाइड ब्रिजिंग.हे चक्रीकरण सिस्टीनच्या अवशेषांच्या जोडीने असुरक्षित केले जाते आणि नंतर डायसल्फाइड बंध तयार करण्यासाठी ऑक्सिडाइझ केले जाते.पॉलीसायक्लिक संश्लेषण सल्फहायड्रिल संरक्षण गट निवडक काढून टाकून प्राप्त केले जाऊ शकते.चक्रीकरण एकतर पोस्ट-डिसोसिएशन सॉल्व्हेंटमध्ये किंवा प्री-डिसोसिएशन राळवर केले जाऊ शकते.रेझिनवरील चक्रीकरण हे सॉल्व्हेंट सायक्लायझेशनपेक्षा कमी प्रभावी असू शकते कारण रेजिनवरील पेप्टाइड्स सहज चक्रीय रचना तयार करत नाहीत.साइड-चेनचा आणखी एक प्रकार - साइड चेन सायक्लायझेशन म्हणजे एस्पार्टिक ऍसिड किंवा ग्लुटामिक ऍसिडचे अवशेष आणि बेस अॅमिनो ऍसिड यांच्यामध्ये अमाइड रचना तयार करणे, ज्यासाठी साइड चेन संरक्षण गट पॉलिपेप्टाइडमधून निवडकपणे काढून टाकण्यास सक्षम असणे आवश्यक आहे. राळ वर किंवा पृथक्करण नंतर.साइड-चेनचा तिसरा प्रकार - साइड चेन सायक्लायझेशन म्हणजे टायरोसिन किंवा पी-हायड्रॉक्सीफेनिलग्लाइसिनद्वारे डायफेनिल इथरची निर्मिती.नैसर्गिक उत्पादनांमध्ये या प्रकारचे चक्रीकरण केवळ सूक्ष्मजीव उत्पादनांमध्ये आढळते आणि सायकलीकरण उत्पादनांमध्ये अनेकदा संभाव्य औषधी मूल्य असते.या संयुगे तयार करण्यासाठी अद्वितीय प्रतिक्रिया परिस्थितीची आवश्यकता असते, म्हणून ते सहसा पारंपारिक पेप्टाइड्सच्या संश्लेषणात वापरले जात नाहीत.
(2) टर्मिनल-टू-साइडचेन
टर्मिनल-साइड चेन सायक्लायझेशनमध्ये सामान्यतः लाइसिन किंवा ऑर्निथिन साइड चेनच्या एमिनो ग्रुपसह सी-टर्मिनल किंवा एस्पार्टिक ऍसिड किंवा ग्लूटामिक ऍसिड साइड चेनसह एन-टर्मिनल समाविष्ट असते.टर्मिनल C आणि सेरीन किंवा थ्रोनाइन साइड चेन यांच्यामध्ये इथर बॉन्ड्स तयार करून इतर पॉलीपेप्टाइड सायकलीकरण केले जाते.
(3) टर्मिनल किंवा हेड-टू-टेल प्रकार
चेन पॉलीपेप्टाइड्स एकतर सॉल्व्हेंटमध्ये सायकल चालवल्या जाऊ शकतात किंवा साखळीच्या साखळी चक्राद्वारे रेझिनवर निश्चित केल्या जाऊ शकतात.पेप्टाइड्सचे ऑलिगोमरायझेशन टाळण्यासाठी पेप्टाइड्सची कमी सांद्रता सॉल्व्हेंट केंद्रीकरणात वापरली पाहिजे.हेड-टू-टेल सिंथेटिक रिंग पॉलीपेप्टाइडचे उत्पादन चेन पॉलीपेप्टाइडच्या अनुक्रमावर अवलंबून असते.म्हणून, मोठ्या प्रमाणावर चक्रीय पेप्टाइड्स तयार करण्यापूर्वी, प्रथम संभाव्य साखळीयुक्त शिशाच्या पेप्टाइड्सची लायब्ररी तयार केली जावी, त्यानंतर सर्वोत्तम परिणामांसह अनुक्रम शोधण्यासाठी सायकलीकरण केले पाहिजे.
2. एन-मेथिलेशन
एन-मेथिलेशन मूळतः नैसर्गिक पेप्टाइड्समध्ये उद्भवते आणि हायड्रोजन बंध तयार होण्यापासून रोखण्यासाठी पेप्टाइड संश्लेषणात आणले जाते, ज्यामुळे पेप्टाइड्स बायोडिग्रेडेशन आणि क्लिअरन्ससाठी अधिक प्रतिरोधक बनतात.N-methylated amino acid डेरिव्हेटिव्ह्ज वापरून पेप्टाइड्सचे संश्लेषण ही सर्वात महत्त्वाची पद्धत आहे.याव्यतिरिक्त, मिथेनॉलसह N- (2-नायट्रोबेन्झिन सल्फोनील क्लोराईड) पॉलीपेप्टाइड-रेसिन इंटरमीडिएट्सची मित्सुनोबू प्रतिक्रिया देखील वापरली जाऊ शकते.ही पद्धत एन-मेथिलेटेड अमीनो ऍसिड असलेली चक्रीय पेप्टाइड लायब्ररी तयार करण्यासाठी वापरली गेली आहे.
3. फॉस्फोरिलेशन
फॉस्फोरिलेशन हे निसर्गातील अनुवादानंतरच्या सर्वात सामान्य बदलांपैकी एक आहे.मानवी पेशींमध्ये, 30% पेक्षा जास्त प्रथिने फॉस्फोरिलेटेड असतात.फॉस्फोरिलेशन, विशेषत: उलट करता येण्याजोगे फॉस्फोरिलेशन, सिग्नल ट्रान्सडक्शन, जनुक अभिव्यक्ती, सेल सायकल आणि सायटोस्केलेटन नियमन आणि एपोप्टोसिस यांसारख्या अनेक सेल्युलर प्रक्रिया नियंत्रित करण्यात महत्त्वाची भूमिका बजावते.
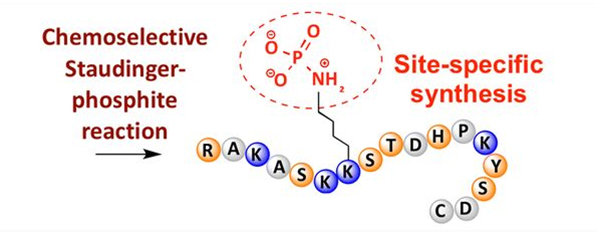
फॉस्फोरिलेशन विविध अमीनो ऍसिडच्या अवशेषांवर पाहिले जाऊ शकते, परंतु सर्वात सामान्य फॉस्फोरिलेशन लक्ष्य म्हणजे सेरीन, थ्रोनिन आणि टायरोसिन अवशेष.फॉस्फोटायरोसिन, फॉस्फोथ्रोनिन आणि फॉस्फोसेरिन डेरिव्हेटिव्ह्ज एकतर संश्लेषणादरम्यान पेप्टाइड्समध्ये येऊ शकतात किंवा पेप्टाइड संश्लेषणानंतर तयार होतात.सेरीन, थ्रोनिन आणि टायरोसिनच्या अवशेषांचा वापर करून निवडक फॉस्फोरिलेशन प्राप्त केले जाऊ शकते जे निवडकपणे संरक्षणात्मक गट काढून टाकतात.काही फॉस्फोरिलेशन अभिकर्मक देखील फॉस्फोरिक ऍसिड गटांना पॉलीपेप्टाइडमध्ये बदल करून टाकू शकतात.अलिकडच्या वर्षांत, लायसिनचे साइट-विशिष्ट फॉस्फोरिलेशन रासायनिक निवडक स्टॉडिंगर-फॉस्फाइट प्रतिक्रिया (आकृती 3) वापरून साध्य केले गेले आहे.
4. मायरीस्टॉयलेशन आणि पामिटायलेशन
फॅटी ऍसिडसह एन-टर्मिनलचे ऍसिलेशन पेप्टाइड्स किंवा प्रथिने पेशींच्या पडद्याला बांधू देते.N-टर्मिनलवरील myridamoylated अनुक्रम Src फॅमिली प्रोटीन किनेसेस आणि रिव्हर्स ट्रान्सक्रिप्टेस गॅक प्रोटीन्सना सेल झिल्लीशी बांधण्यासाठी लक्ष्यित करण्यास सक्षम करते.मायरिस्टिक ऍसिड हे मानक कपलिंग प्रतिक्रियांचा वापर करून रेझिन-पॉलीपेप्टाइडच्या एन-टर्मिनलशी जोडलेले होते आणि परिणामी लिपोपेप्टाइड मानक परिस्थितीत वेगळे केले जाऊ शकते आणि RP-HPLC द्वारे शुद्ध केले जाऊ शकते.
5. ग्लायकोसिलेशन
ग्लायकोपेप्टाइड्स जसे की व्हॅनकोमायसिन आणि टेकोलानिन हे औषध-प्रतिरोधक बॅक्टेरियाच्या संसर्गाच्या उपचारांसाठी महत्वाचे प्रतिजैविक आहेत आणि इतर ग्लायकोपेप्टाइड्सचा वापर रोगप्रतिकारक शक्तीला उत्तेजन देण्यासाठी केला जातो.याव्यतिरिक्त, अनेक सूक्ष्मजीव प्रतिजन ग्लायकोसिलेटेड असल्याने, संक्रमणाचा उपचारात्मक प्रभाव सुधारण्यासाठी ग्लायकोपेप्टाइड्सचा अभ्यास करणे खूप महत्वाचे आहे.दुसरीकडे, असे आढळून आले आहे की ट्यूमर पेशींच्या पेशीच्या पडद्यावरील प्रथिने असामान्य ग्लायकोसिलेशन प्रदर्शित करतात, ज्यामुळे ग्लायकोपेप्टाइड्स कर्करोग आणि ट्यूमर रोगप्रतिकारक संरक्षण संशोधनात महत्त्वपूर्ण भूमिका बजावतात.ग्लायकोपेप्टाइड्स Fmoc/t-Bu पद्धतीने तयार केले जातात.ग्लायकोसिलेटेड अवशेष, जसे की थ्रोनिन आणि सेरीन, ग्लायकोसिलेटेड एमिनो ऍसिडचे संरक्षण करण्यासाठी पेंटाफ्लोरोफेनॉल एस्टर सक्रिय एफएमओसीद्वारे पॉलीपेप्टाइड्समध्ये प्रवेश करतात.
6. आयसोप्रीन
सी-टर्मिनलजवळील बाजूच्या साखळीतील सिस्टीन अवशेषांवर आयसोपेन्टाडायनायलेशन होते.प्रथिने आयसोप्रीन सेल झिल्लीची आत्मीयता सुधारू शकते आणि प्रथिने-प्रथिने परस्परसंवाद तयार करू शकते.आयसोपेंटेडिएनेटेड प्रथिनांमध्ये टायरोसिन फॉस्फेटस, लहान GTase, कोकापेरोन रेणू, न्यूक्लियर लॅमिना आणि सेंट्रोमेरिक बंधनकारक प्रथिने यांचा समावेश होतो.आयसोप्रीन पॉलीपेप्टाइड्स रेझिन्सवर आयसोप्रीन वापरून किंवा सिस्टीन डेरिव्हेटिव्ह्ज सादर करून तयार केले जाऊ शकतात.
7. पॉलिथिलीन ग्लायकॉल (पीईजी) बदल
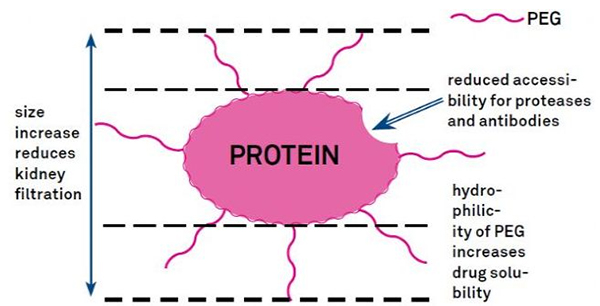
प्रथिने हायड्रोलाइटिक स्थिरता, जैव वितरण आणि पेप्टाइड विद्राव्यता सुधारण्यासाठी पीईजी बदलाचा वापर केला जाऊ शकतो.पेप्टाइड्सना PEG चेनचा परिचय करून दिल्याने त्यांचे औषधी गुणधर्म सुधारू शकतात आणि प्रोटीओलाइटिक एन्झाईम्सद्वारे पेप्टाइड्सचे हायड्रोलिसिस देखील रोखू शकतात.पीईजी पेप्टाइड्स ग्लोमेरुलर केशिका क्रॉस सेक्शनमधून सामान्य पेप्टाइड्सपेक्षा अधिक सहजतेने जातात, ज्यामुळे रेनल क्लिअरन्स मोठ्या प्रमाणात कमी होते.विवोमधील पीईजी पेप्टाइड्सच्या वाढीव सक्रिय अर्धायुष्यामुळे, कमी डोस आणि कमी वारंवार पेप्टाइड औषधांनी सामान्य उपचार पातळी राखली जाऊ शकते.तथापि, पीईजी सुधारणेचे नकारात्मक परिणाम देखील आहेत.मोठ्या प्रमाणात पीईजी एन्झाईमला पेप्टाइड खराब होण्यापासून प्रतिबंधित करते आणि पेप्टाइडचे टार्गेट रिसेप्टरचे बंधन कमी करते.परंतु पीईजी पेप्टाइड्सची कमी आत्मीयता सहसा त्यांच्या दीर्घ फार्माकोकिनेटिक अर्धायुष्यामुळे भरून काढली जाते आणि शरीरात जास्त काळ उपस्थित राहिल्याने, पीईजी पेप्टाइड्सचे लक्ष्य ऊतींमध्ये शोषले जाण्याची अधिक शक्यता असते.म्हणून, पीईजी पॉलिमर तपशील इष्टतम परिणामांसाठी अनुकूल केले पाहिजेत.दुसरीकडे, रेनल क्लिअरन्स कमी झाल्यामुळे पीईजी पेप्टाइड्स यकृतामध्ये जमा होतात, परिणामी मॅक्रोमोलेक्युलर सिंड्रोम होतो.म्हणून, जेव्हा औषध चाचणीसाठी पेप्टाइड्सचा वापर केला जातो तेव्हा पीईजी सुधारणा अधिक काळजीपूर्वक डिझाइन करणे आवश्यक आहे.
पीईजी मॉडिफायर्सचे सामान्य बदल गट साधारणपणे खालीलप्रमाणे सारांशित केले जाऊ शकतात: Amino (-amine) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimide कार्बोनेट - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (जसे की propional-ald, butyrALD), ऍक्रेलिक बेस (-acrylate-acrl), azido-azide, बायोटिन, फ्लोरेसिन, ग्लूटेरिल -जीए, ऍक्रिलेट हायड्राझाइड, अल्काइन-अल्काइन, पी-टोल्युनेसल्फोनेट -ओटी, ससिनिमाइड सक्सीनेट -एसएस, इ. कार्बोक्झिलिक ऍसिडसह पीईजी डेरिव्हेटिव्ह्ज एन-टर्मिनल अमाइन किंवा लिसिन साइड चेनमध्ये जोडले जाऊ शकतात.एमिनो-सक्रिय PEG एस्पार्टिक ऍसिड किंवा ग्लूटामिक ऍसिड साइड चेनमध्ये जोडले जाऊ शकते.माल-सक्रिय PEG पूर्णपणे असुरक्षित सिस्टीन साइड चेन [११] च्या मर्कॅप्टनशी संयुग्मित केले जाऊ शकते.PEG मॉडिफायर्सचे सामान्यतः खालीलप्रमाणे वर्गीकरण केले जाते (टीप: mPEG हे methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH आहे):
(1) सरळ साखळी PEG सुधारक
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) द्विकार्यात्मक PEG सुधारक
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) शाखा पीईजी सुधारक
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. बायोटिनायझेशन
बायोटिन हे एव्हिडिन किंवा स्ट्रेप्टाव्हिडिनशी जोरदारपणे बांधले जाऊ शकते आणि बंधनकारक शक्ती सहसंयोजक बंधाच्या अगदी जवळ असते.बायोटिन-लेबल केलेले पेप्टाइड्स सामान्यतः इम्युनोसे, हिस्टोसाइटोकेमिस्ट्री आणि फ्लोरोसेन्स-आधारित फ्लो सायटोमेट्रीमध्ये वापरले जातात.लेबल केलेल्या प्रतिजैविक प्रतिपिंडांचा वापर बायोटिनिलेटेड पेप्टाइड्स बांधण्यासाठी देखील केला जाऊ शकतो.बायोटिन लेबले बहुधा लाइसिन साइड चेन किंवा एन टर्मिनलशी संलग्न असतात.6-अमीनोकाप्रोइक ऍसिड बहुतेकदा पेप्टाइड्स आणि बायोटिन यांच्यातील बंधन म्हणून वापरले जाते.बॉण्ड सब्सट्रेटला बांधण्यासाठी लवचिक असतो आणि स्टेरिक अडथळाच्या उपस्थितीत अधिक चांगले बांधतो.
9. फ्लोरोसेंट लेबलिंग
फ्लूरोसंट लेबलिंगचा उपयोग जिवंत पेशींमध्ये पॉलीपेप्टाइड्स शोधण्यासाठी आणि एन्झाईम्स आणि कृतीच्या यंत्रणेचा अभ्यास करण्यासाठी केला जाऊ शकतो.ट्रिप्टोफॅन (Trp) फ्लोरोसेंट आहे, म्हणून ते आंतरिक लेबलिंगसाठी वापरले जाऊ शकते.ट्रायप्टोफनचे उत्सर्जन स्पेक्ट्रम परिघीय वातावरणावर अवलंबून असते आणि कमी होत असलेल्या सॉल्व्हेंट पोलॅरिटीसह कमी होते, एक गुणधर्म जी पेप्टाइड संरचना आणि रिसेप्टर बंधन शोधण्यासाठी उपयुक्त आहे.प्रोटोनेटेड एस्पार्टिक ऍसिड आणि ग्लूटामिक ऍसिडद्वारे ट्रिप्टोफॅन फ्लूरोसेन्स शमन केले जाऊ शकते, ज्यामुळे त्याचा वापर मर्यादित होऊ शकतो.डॅन्सिल क्लोराईड गट (डॅन्सिल) अमीनो गटाशी बांधलेला असताना अत्यंत फ्लोरोसेंट असतो आणि बहुतेकदा अमीनो ऍसिड किंवा प्रथिनांसाठी फ्लोरोसेंट लेबल म्हणून वापरला जातो.
फ्लूरोसेन्स रेझोनान्स एनर्जी कन्व्हर्जन (FRET) हे एन्झाइम अभ्यासासाठी उपयुक्त आहे.जेव्हा FRET लागू केले जाते, तेव्हा सब्सट्रेट पॉलीपेप्टाइडमध्ये सामान्यतः फ्लूरोसेन्स-लेबलिंग ग्रुप आणि फ्लूरोसेन्स-क्वेंचिंग ग्रुप असतो.लेबल केलेले फ्लोरोसेंट गट क्वेन्चरद्वारे नॉन-फोटॉन ऊर्जा हस्तांतरणाद्वारे शमन केले जातात.जेव्हा पेप्टाइड प्रश्नातील एंझाइमपासून वेगळे केले जाते, तेव्हा लेबलिंग गट फ्लोरोसेन्स उत्सर्जित करतो.
10. पिंजरा पॉलीपेप्टाइड्स
केज पेप्टाइड्समध्ये ऑप्टिकली काढता येण्याजोगे संरक्षणात्मक गट असतात जे पेप्टाइडला रिसेप्टरला बांधण्यापासून वाचवतात.अतिनील किरणोत्सर्गाच्या संपर्कात आल्यावर, पेप्टाइड सक्रिय होते, रिसेप्टरशी त्याची आत्मीयता पुनर्संचयित करते.कारण हे ऑप्टिकल सक्रियकरण वेळ, मोठेपणा किंवा स्थानानुसार नियंत्रित केले जाऊ शकते, पिंजरा पेप्टाइड्सचा वापर पेशींमध्ये होणाऱ्या प्रतिक्रियांचा अभ्यास करण्यासाठी केला जाऊ शकतो.केज पॉलीपेप्टाइड्ससाठी सर्वात सामान्यतः वापरले जाणारे संरक्षणात्मक गट 2-नायट्रोबेंझिल गट आणि त्यांचे डेरिव्हेटिव्ह आहेत, जे पेप्टाइड संश्लेषणात संरक्षणात्मक अमीनो ऍसिड डेरिव्हेटिव्हद्वारे सादर केले जाऊ शकतात.एमिनो ऍसिड डेरिव्हेटिव्ह जे विकसित केले गेले आहेत ते लाइसिन, सिस्टीन, सेरीन आणि टायरोसिन आहेत.एस्पार्टेट आणि ग्लूटामेट डेरिव्हेटिव्ह्ज, तथापि, पेप्टाइड संश्लेषण आणि पृथक्करण दरम्यान त्यांच्या चक्रीयतेच्या संवेदनाक्षमतेमुळे सामान्यतः वापरले जात नाहीत.
11. पॉलींटिजेनिक पेप्टाइड (MAP)
लहान पेप्टाइड्स सहसा रोगप्रतिकारक नसतात आणि प्रतिपिंड तयार करण्यासाठी वाहक प्रथिनांशी जोडले जाणे आवश्यक आहे.पॉलींटिजेनिक पेप्टाइड (MAP) हे लाइसिन न्यूक्लीशी जोडलेल्या अनेक एकसारख्या पेप्टाइड्सचे बनलेले असते, जे विशेषत: उच्च सामर्थ्य इम्युनोजेन्स व्यक्त करू शकतात आणि पेप्टाइड-वाहक प्रथिने जोड तयार करण्यासाठी वापरले जाऊ शकतात.MAP पॉलीपेप्टाइड्स MAP राळ वर घन फेज संश्लेषणाद्वारे संश्लेषित केले जाऊ शकतात.तथापि, अपूर्ण जोडणीमुळे काही शाखांवरील पेप्टाइड चेन गहाळ किंवा कापल्या जातात आणि त्यामुळे मूळ MAP पॉलीपेप्टाइडचे गुणधर्म प्रदर्शित होत नाहीत.पर्याय म्हणून, पेप्टाइड्स स्वतंत्रपणे तयार आणि शुद्ध केले जाऊ शकतात आणि नंतर MAP मध्ये जोडले जाऊ शकतात.पेप्टाइड कोरशी जोडलेला पेप्टाइड अनुक्रम चांगल्या प्रकारे परिभाषित केला जातो आणि मास स्पेक्ट्रोमेट्रीद्वारे सहजपणे दर्शविला जातो.
निष्कर्ष
पेप्टाइड मॉडिफिकेशन हे पेप्टाइड्स डिझाइन करण्याचे एक महत्त्वाचे साधन आहे.रासायनिक सुधारित पेप्टाइड्स केवळ उच्च जैविक क्रियाकलाप राखू शकत नाहीत, तर इम्युनोजेनिकता आणि विषारीपणाचे दोष प्रभावीपणे टाळतात.त्याच वेळी, रासायनिक बदल काही नवीन उत्कृष्ट गुणधर्मांसह पेप्टाइड्स प्रदान करू शकतात.अलिकडच्या वर्षांत, पॉलीपेप्टाइड्सच्या पोस्ट-फेरफारसाठी सीएच सक्रियकरणाची पद्धत वेगाने विकसित केली गेली आहे आणि अनेक महत्त्वपूर्ण परिणाम प्राप्त झाले आहेत.
पोस्ट वेळ: मार्च-20-2023
